Công nghệ Ozone
Yếu tố ảnh hưởng đến quá trình phân hủy của ozone trong nước và không khí
Khi ozone được sinh ra, chúng nhanh chóng bị phân hủy trong thời gian ngắn bởi đây là một hợp chất có liên kết kém bền vững. Sự phân hủy của ozone không chỉ phụ thuộc vào nhiệt độ môi trường mà chúng còn bị ảnh hưởng bởi nồng độ pH, nồng độ các chất hòa tan, các chất hữu cơ tự nhiên. Cụ thể như sau:
Nhiệt độ
Nhiệt độ có ảnh hưởng quan trọng đến thời gian phân rã của ozone. Bảng dưới đây cho thấy, với những nền nhiệt độ khác nhau, thời gian tồn tại của ozone trong nước và không khí là khác nhau. Ngoài ra, ozone trong nước cũng phân hủy nhanh hơn khi chúng tồn tại trong môi trường không khí.
| Không khí | Nước (pH=7) | ||
| Nhiệt độ (0C) | Thời gian tồn tại | Nhiệt độ (0C) | Thời gian tồn tại |
| -50 | 3 tháng | 15 | 30 phút |
| -35 | 18 ngày | 20 | 20 phút |
| -25 | 8 ngày | 25 | 15 phút |
| 20 | 3 ngày | 30 | 12 phút |
| 120 | 1,5 giờ | 35 | 8 phút |
| 250 | 1,5 giây | ||
Nồng độ pH
Trong điều kiện nước có nồng độ pH nằm trong khoảng từ 6 đến 8.5, một phần của chúng phản ứng với các gốc OH tự do (OH-). Do đó, khi giá trị pH tăng lên, các OH- cũng tăng, dẫn đến hàm lượng ion hydroxit tăng cao. Các ion hydroxit hoạt động như một chất khởi đầu của sự phân rã ozone. Các phương trình diễn ra như sau:
O3 + OH- à HO2– + O2
O3 + HO2– à OH- + O2 + O2–
Các gốc tự do được sinh ra trong các phản ứng trên có thể tạo thành các phản ứng khác với ozone. Kết quả là nhiều gốc OH- được hình thành.
Ngoài ra, nồng độ pH còn ảnh hưởng đến sự cân bằng các acid, bazo của một số hợp chất cũng như tốc độ phản ứng của ozone.
Hình dưới đây thể hiện tốc độ phân rã của ozone trong môi trường axit (nhiệt độ 150C) là thấp hơn so với môi trường cơ bản.
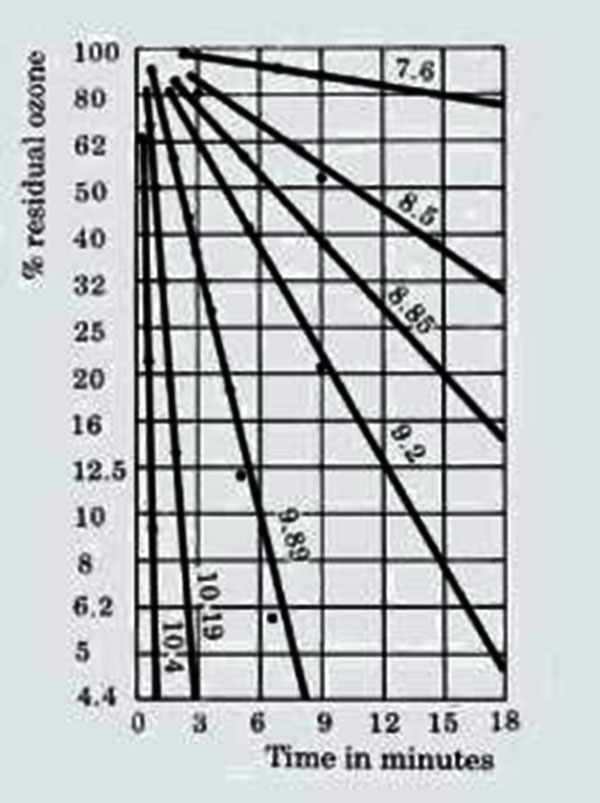
Nồng độ chất rắn hòa tan
Ozone có thể phản ứng với nhiều chất rắn hòa tan khác nhau như: Hợp chất hữu cơ, vi khuẩn, virus, … để tạo thành các chất khác.
Trong một thí nghiệm về tốc độ phân rã của ozone với các loại nước khác nhau (Nước cất 2 lần, nước cất 1 lần, nước máy, nước ngầm có độ cứng thấp, nước lọc từ hồ Zurich- Thụy Sỹ, nước lọc từ Bodensee- Thụy Sỹ) trong nền nhiệt 200C đã chứng minh rằng: Tốc độ phân hủy ozone trong nước cất ngắn hơn so với nước khai thác trong tự nhiên. Kết quả được thể hiện trong biểu đồ dưới đây:
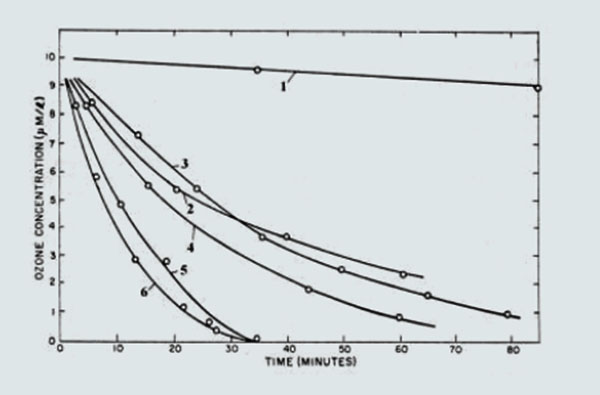
Sự phân hủy của ozone đối với các gốc OH tự do trong nước phụ thuộc vào chất xúc tác, chúng có thể kích thích hoặc làm chậm sự quá trình phân rã. Khi đó, các chất thúc đẩy quá trình được gọi là các chất xúc tác và chất làm chậm phản ứng gọi là chất ức chế. Chất ức chế là các đơn vị phản ứng với OH gốc tự do.
Carbonate và Bicarbonate
Carbonate là một chất ức chế mạnh mẽ, việc bổ sung cacbonat (CO32-) có thể khiến chu trình phân hủy của ozone diễn ra lâu hơn. Khi một phản ứng gián tiếp xảy ra (Phản ứng với gốc OH-) chúng sẽ làm tăng sự hiện diện của các chất ức chế. Các chất ức chế tác dụng với gốc OH- và làm giảm khả năng oxy hóa.
So với cacbonat, các ion bicarbonate (HCO32-) khiến quá trình phân hủy của ozone diễn ra nhanh hơn (Tốc độ phản ứng của CO32- là 4,2*108 M-1s-1; tốc độ phản ứng của HCO3- là 1.5*1-7 M-1s-1). Do đó, khi ozone hóa nước uống, nồng độ Bicarbonate là ít quan trọng. Biểu đồ dưới đây thể hiện mối quan hệ giữa cacbonat, tie lệ Bicarbonate và pH để chứng minh điều này.
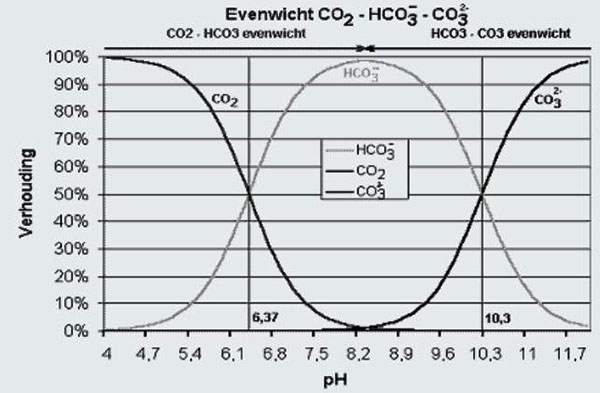
Vật liệu hữu cơ tự nhiên (NOM)
Vật liệu hữu cơ tự nhiên tồn tại trong tất cả các loại nước có nguồn gốc tự nhiên và thường được đo bằng carbon hữu cơ hòa tan (DOC), chúng ảnh hưởng đến màu sắc và mùi vị của nước.
Máy tạo ozone có thể được sử dụng để xử lý nước và làm giảm nồng độ của NOM. Khi ozone sục vào trong nước, chúng tác dụng trực tiếp với các vật liệu hữu cơ tự nhiên (Hợp chất hữu cơ thơm, các amin deprotonated, sunfua) hoặc phản ứng gián tiếp (thông qua các OH-). Mặc dù vậy, trong nước tự nhiên, rất khó để xác định được độ ổn định của ozone cũng như các yếu tố ảnh hưởng đến quá trình phản ứng nhanh, chậm của chúng.

